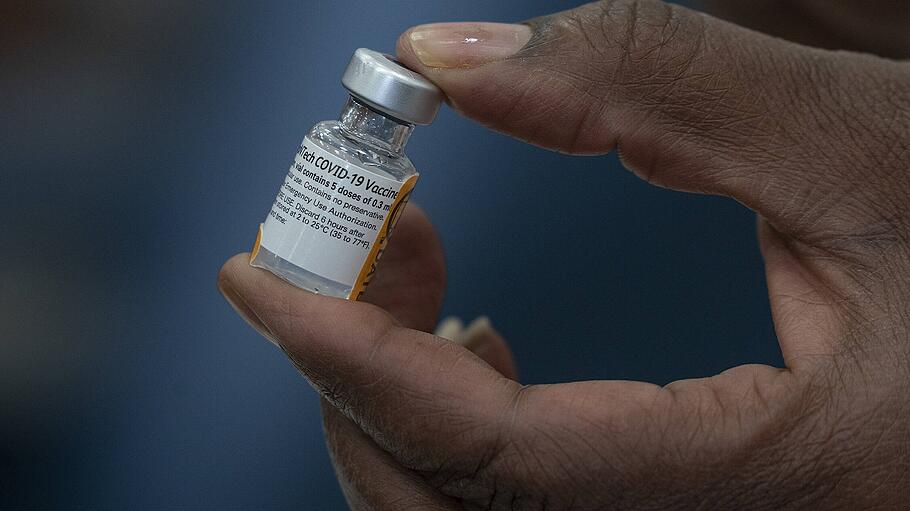
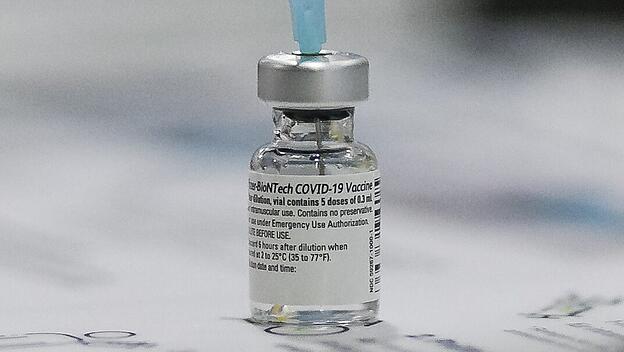
In den Vereinigten Staaten haben die Impfungen mit dem mRNA-Impfstoff BNT162b2 begonnen. Die Frucht der Kooperation des Mainzer Unternehmens Biontech mit dem US-amerikanischen Pharmakonzern Pfizer hatte vergangene Woche dort eine Notfallzulassung erhalten. Und auch in Großbritannien wird das Vakzin bereits verabreicht. Das erhöht selbstverständlich den ohnehin starken Druck auf die Europäische Arzneimittelagentur EMA, BNT162b2 nun auch für Europa zuzulassen.
Die EMA verlangt mehr Daten
Die EMA tut gut daran, diesem Druck standzuhalten. Niemand kann ihr die Verantwortung abnehmen, die vorhandenen Daten selbst eingehend und sorgfältig zu prüfen. Statt über die Brüsseler Bürokraten die Nase zu rümpfen, sollten die Bürger der Mitgliedsstaaten der Europäischen Union dankbar sein, dass die EMA von den Herstellern mehr und genauere Daten über die Nebenwirkungen des Impfstoffes verlangt, als dies in Großbritannien und den USA der Fall ist. In Großbritannien hat die zuständige Behörde nach den ersten Erfahrungen, nun Allergikern bereits von einer Impfung mit BNT162b2 abgeraten.
„Einfach mal machen“, ist eben keine gute Idee, wenn ein Medizinprodukt nach einem völlig neuen Verfahren in Windeseile entwickelt und in Studien getestet wird, die erst vor fünf Monaten gestartet wurden. In der Europäischen Union leben 446 Millionen Menschen, nur in China und Indien sind es mehr. Als Vorbilder für die Verantwortung, die Behörden bei Entscheidungen zukommen, die sämtliche Bürger eines Gemeinwesens betreffen, taugen sie allenfalls begrenzt.
Die Printausgabe der Tagespost vervollständigt aktuelle Nachrichten auf die-tagespost.de mit Hintergründen und Analysen.